在神经科学限制,参谋者恒久濒临一个瓶颈:天然现存技能好像监测神经元发出的电信号(输出),却难以径直不雅测神经元给与的化学信号(输入)。
这就像只可通过听一个东谈主说的话来臆测他的思法,却无法得知他听到了什么、是什么影响了他的回话。这种对突触输入信号给与与整合进程的不见解性,一直甘休着咱们对大脑信息贬责根蒂机制的意会。
12 月 23 日,针对这一问题,来自艾伦参谋所(Allen Institute)和霍华德·休斯医学参谋所(HHMI)珍利亚参谋园区的鸠合团队,在 Nature Methods 期刊上发表了一项具有里程碑意旨的驱散。
他们得胜研发出第四代遗传编码谷氨酸指令剂——iGluSnFR4。

图 | 团队论文:《具有更高理智度和定制失活速率的谷氨酸指令剂》(开始:Nature Methods)
这是一种新式的卵白质传感器。使用它,如同为大脑植入了一套高理智度的“窃听安设”,使科学家初度能了了、及时地捕捉神经元给与信息的转眼,况且看清关节的谷氨酸化学信号。
由于谷氨酸信号传递的巨大是阿尔茨海默病、精神分裂症等神经系统疾病的中枢款式之一。这一冲突关于它们的病理分析有着巨大匡助。
在此之前,神经科学参谋主要依赖钙离子指令剂或电压指令剂来记载神经步履。这些器用天然强盛,但它们捕捉的不息是神经元整合信息后的“驱散”——即当作电位或与之干系的钙涌流。
然而,大脑的缱绻中枢其简直于“进程”。数以千计的突触前神经元开释神经递质谷氨酸,这些化学信号最初突触破绽,作用于突触后膜,经过极其复杂的非线性整合,最终才决定了一个神经元是否放电。
在这个微不雅步履上,旧有的技能显得前门去虎,前门拒虎:要么反应太慢,无法分辨快速一语气的信号;要么理智度太低,褪色在配景杂音中;要么因为过快的光漂白,绮丽了荧光卵白的神经元跟着激光照耀,产生损耗变暗,而无法进行万古程不雅测。
为了攻克“看得慢”又“看不清”的两浩劫题,由卡斯帕·波德戈尔斯基(Kaspar Podgorski)博士和杰里米·哈塞曼(Jeremy Hasseman)博士指令的团队,对早期的谷氨酸传感器进行了澈底的基因工程改良。
参谋团队不再追求一个万能的传感器,而是主动瞎想出具有不同性能侧要点的专用器用。由于传感器的速率(团结与开释谷氨酸的快慢)和理智度(信号亮度)在分子结构上不息此消彼长。
于是,他们选用了组合突变筛选战略,像系统性地休养钟表的齿轮相通,对卵白质中影响其能源学特质的关节区域进行了数千种基因改良,并在培养皿中逐个测试这些变体的性能。
最终,他们锁定了两款性能迥异但互补的中枢器用:iGluSnFR4f 和 iGluSnFR4s。
这里的后缀“f”代表快速(fast),而“s”代表慢速(slow)。
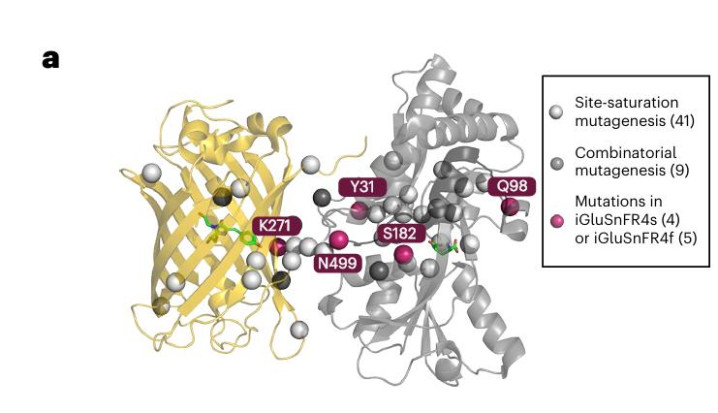
iGluSnFR4f 是为了极致的速率而生,它的失活期间常数仅为 26 毫秒。在小鼠的低级视觉皮层试验中,参谋东谈主员运用双光子显微镜不雅察到,当小鼠受到视觉刺激时,这款传感器好像以极高的期间分辨率,了了地分辨出单个突触上一语气发生的谷氨酸开释事件。
即使是在以 100 赫兹的高频进行一语气成像时,它照旧能保抓了了的信号轨迹,莫得出现信号混叠。关于那些需要参谋神经编码精确期间特质的试验来说,这无疑是一把明锐的手术刀。
比较之下,iGluSnFR4s则走了一条不同的道路。它的失活期间较长,约为 153 毫秒,这使得它好像整合更多的光子,从而产生更亮堂的荧光信号。
这种高理智度使其成为不雅测隐微信号或进行大规模群体记载的理思遴荐。
在针对腹侧被盖区(VTA)多巴胺能神经元的参谋中,科学家运用光纤光度法(Fiber Photometry)互助 iGluSnFR4s,得胜记载到了与赏赐步履高度干系的群体谷氨酸信号波动。
其试验数据披露,其信噪比是上一代传感器 iGluSnFR3 的数倍,这意味着参谋者不错用更低的光功率赢得更了了的数据,极地面缩小了光毒性对脑组织的损害。
这项技能让“看不见”酿成了“了了可见”。
在显微镜下,这些被绮丽的神经元树突棘不再是静止的结构,而是跟着信息的流入闪耀着后光,如同夜空中的点点繁星。
艾伦参谋所的波德戈尔斯基博士用一个无邪的比方状貌这一冲突:“以前,咱们就像在读一册单词被十足打乱的书,根蒂无法意会句子的结构和含义。当今,咱们终于把单词之间的畅通线画了出来,意会了它们陈设的礼貌,也就读懂了大脑本来思要抒发的故事。”
为了考据这套器用在活体动物中的骨子遵循,参谋团队在小鼠的触须桶状皮层(Barrel Cortex)进行了一系列严苛的测试。
家喻户晓,啮齿类动物通过快速舞动触须来感知宇宙,这种感官输入的频率极高,对传感器的反应速率提倡了巨大挑战。试验驱散披露,iGluSnFR4f 展现出了惊东谈主的动态捕捉才气。
当小鼠摆脱挥动触须触碰物体时,传感器精确地记载下了每一次触碰激发的谷氨酸开释,即就是远离极短的一语气触碰也能被了了辞别。而在昔时,这类高频信号不息会被旧型传感器暗昧成一团无法领会的抓续光斑。
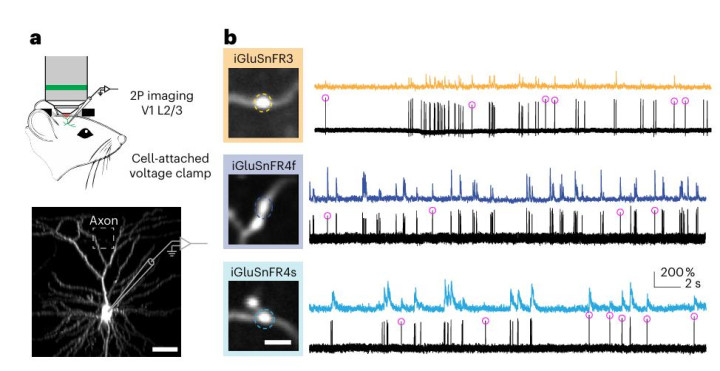
图 | 小鼠视觉皮层中iGluSnFR4的表征 (开始:论文)
更令东谈主兴盛的是,这项技能揭示了大脑贬责信息时的空间特异性。在视觉皮层的试验中,参谋东谈主员发现,褪色根树突上的不同棘突(Spine)会对不同地方的确认光栅产生反应。
获利于新器用的高信噪比和低配景杂音,科学家们不仅能看到哪些棘突在活跃,还能精笃定位它们的空间漫步,以致不雅察到相邻突触之间是若何保抓功能寥寂的。这种在单突触分辨率下进行的“功能性畅通组学”参谋,在此前险些是不成思象的。
天然,从试验室的培养皿到复杂的活体大脑,每一步最初齐充满了挑战。研发团队在筛选进程中不仅要筹商传感器的亮度与速率,还要兼顾其在膜名义的抒发水平以及对泛泛生理进程的烦嚣。
他们发现,通过引入特定的膜定位序列(如NGR序列),不错将这些传感器更精确地锚定在突触后膜的名义,径直面对突触破绽中开释的谷氨酸激流。这种分子层面的小巧瞎想,确保了传感器既能明锐捕捉信号,又不会因为过度霸占受体而影响神经元泛泛的突触传递。
这一器用的问世,其影响远不啻于基础神经科学限制。关于药物研发而言,它提供了一个全新的筛选平台。很多神经精神类疾病,如抑郁症、自闭症和癫痫,齐被以为与谷氨酸信号系统的失调相关。
昔时,药企在筛选新药时,不息只可通过不雅察细胞厌世率或合座电生理变化来评估药效,这些主见既宏不雅又滞后。
而当今,运用 iGluSnFR4,研发东谈主员不错径直不雅察药物分子若何影响突触层面的谷氨酸传递效率。这就配备了一副高倍千里镜,让他们能径直看到药物是否击中了靶心。
参考贵寓
论文地址:10.1038/s41592-025-02965-z
运营/排版:何晨龙